Qu'est-ce que la galvanisation à chaud ?
1. Introduction
La galvanisation à chaud des alliages ferreux est une opération de revêtement par trempé dans un bain de zinc ou d'alliage de zinc en fusion à une température voisine de 460° C. Elle concerne les pièces finies (par exemple : tirefonds), pour la « galvanisation à chaud au trempé », les tôles (cavaliers, plaquettes) et les fils revêtus (tiges et crochets), pour la « galvanisation à chaud en continu ».
Le mot « galvanisation » est souvent employé à tort, l'effet galvanique pouvant s'appliquer aux autres applications du zinc, (shérardisation, zin gage électrolytique...). L'ambiguïté sur le mot « galvanisation » a conduit à de nombreux problèmes d'interprétation, et la norme française NFA 91-010 interdit l'emploi du mot « galvanisé » lorsqu'il s'agit de pièces électrozinguées (le terme « galvanisation à chaud » est réservé exclusivement au recouvrement par « immersion dans un bain de zinc fondu »).

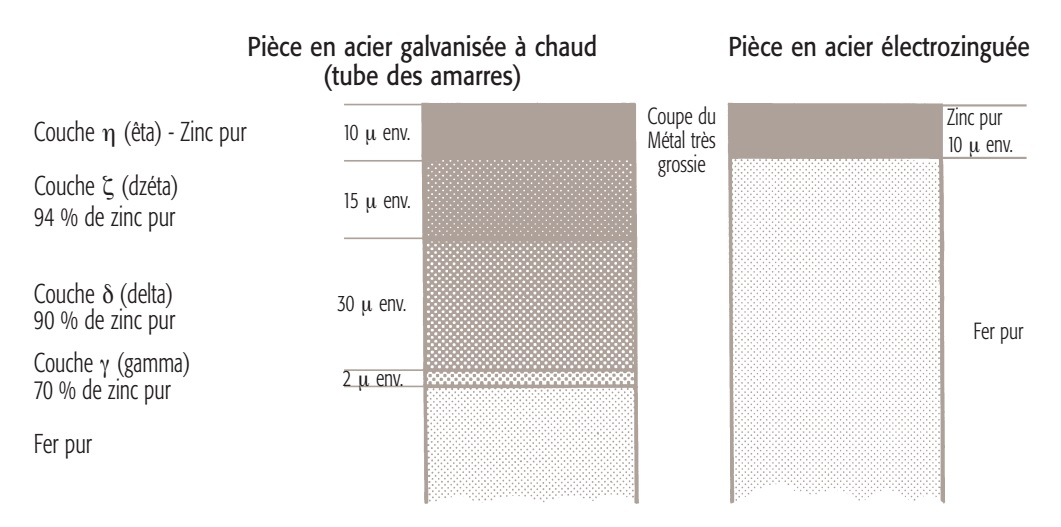
La galvanisation à chaud est un procédé de revê- tement (traitement de surface) anticorrosion traditionnel. Ce traitement n'en est pas moins efficace ! !
En effet, un des principaux avantages du zinc est sa grande électronégativité par rapport à celle de l'acier : il sert ainsi à la protection électrochimique de l'acier contre la corrosion.
2. Protection électrochimique par galvanisation
La corrosion est la résultante de réactions électrochimiques dues à la formation de piles locales. Il faut 4 éléments pour les former :
– un électrolyte (eau, sol...),
– deux électrodes à potentiels différents,
– une connexion électrique.
L'électrode ayant le potentiel le plus électronéga tif est appelée anode. C'est elle qui subit les phénomènes d'oxydation (perte d'électrons) donc de corrosion.
L'électrode ayant le potentiel le moins électronégatif est la cathode, où se passe des phénomènes de réduction (gain d'électrons) donc de protection.
Dans le cas d'une pièce en acier galvanisée, les matériaux acier – zinc forment une pile électrochimique où l'acier est la cathode et le zinc l'anode. (Potentiel du fer = – 0,44V et potentiel du zinc = – 0,76V).
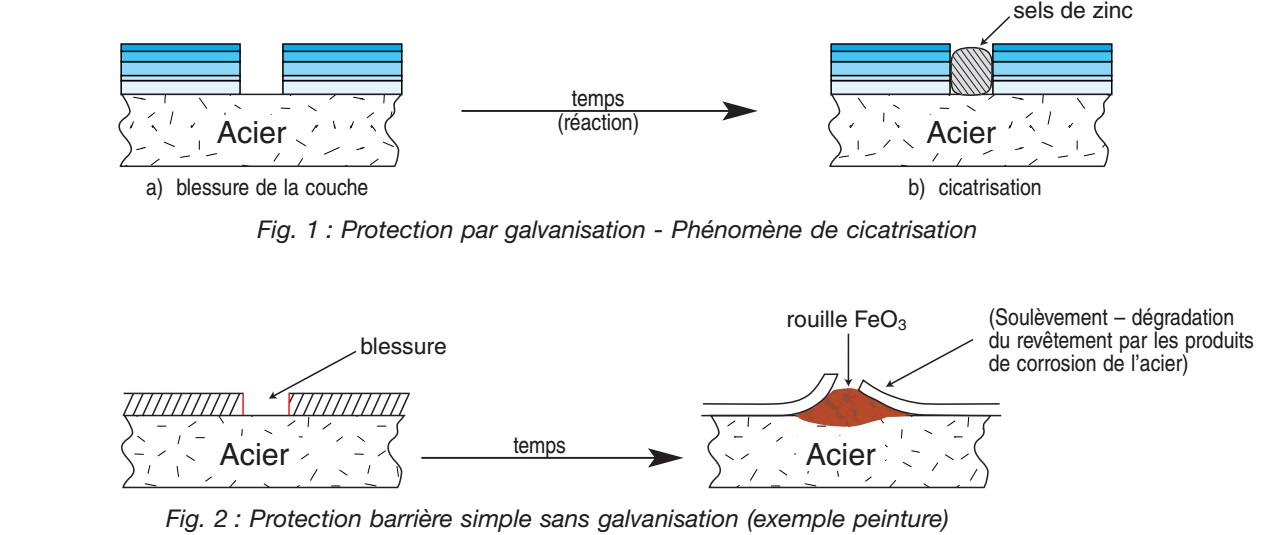
L'acier sera protégé par le zinc qui se dissoudra dans une réaction cathodique lente. L'attaque du zinc (perte d'électrons, ou oxydation Zn → Zn2+ +2e–) se fera avec la formation d'oxydes, d'hydroxydes, d'hydrocarbonate, etc., sels à carac tère protecteur conduisant à une cicatrisation locale de la détérioration de l'acier qui n’est pas recouvert (figure 1).
A cette protection électrochimique s'ajoute bien évidemment la protection physico-chimique (ou protection barrière) que confère une couche sur une surface (comme une peinture, métal...).
Une seule couche de peinture ne permet pas une protection électrochimique : il y aura, si la surface de revêtement n'est pas continue (ou si elle est blessée), une formation de rouille, donc soulèvement – dégradation du revêtement par la rouille (Fe O3) (figure 2)
3. Influence de l'épaisseur du traitement :
La durée de protection contre la corrosion assu rée par galvanisation (soit gris clair, soit gris foncé) est approximativement proportionnelle à l'épaisseur du revêtement.
Généralement, on parle pour déterminer l'épais seur en terme de gramme/m2 (masse déposée).
4. Différentes galvanisations à chaud :
Il y a essentiellement :
– La galvanisation à chaud au trempé.
Chaque fois que l'on recherche une bonne protection contre la corrosion et que le fini des surfaces (aspect esthétique) ne requiert pas de conditions spécifiques, on peut appliquer la galvanisation à chaud au trempé. Les qualités et les caractéristiques du développement sont essentiellement fonction de la composition de l'acier, de la composition et la température du bain de zinc, de la durée d'immersion... Notons qu'une bonne galvanisation ne peut s'obtenir qu'avec une préparation de surface de l'acier adaptée.
Les épaisseurs de zinc par galvanisation à chaud au trempé sont plus importantes que les autres procédés de galvanisation.
– La galvanisation en continu des tôles.
Les principales caractéristiques des revêtements de tôles galvanisées sont regroupées dans le tableau ci-après (d'après les normes NF EN 10346
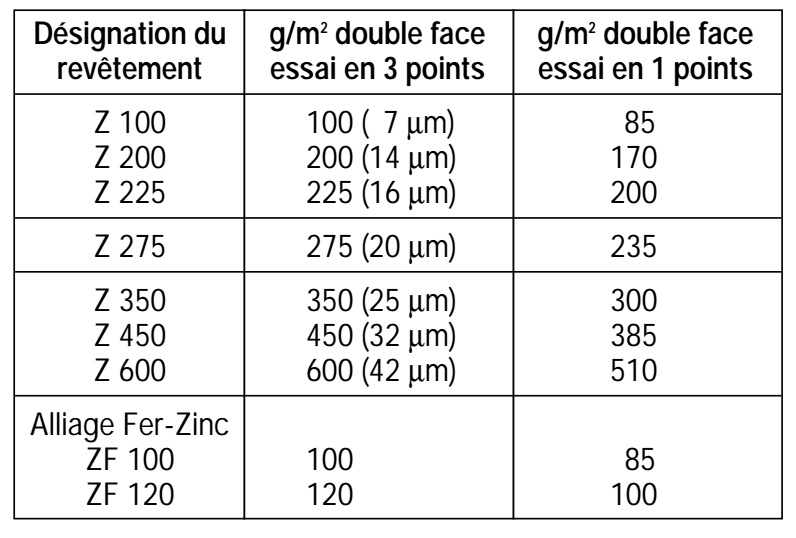
Il existe également des lignes de prélaquage en continu couplées à la ligne de galvanisation, ce qui permet une protection supplémentaire (protection barrière supplémentaire), et un aspect esthétique varié (différentes couleurs).
– La galvanisation des fils.
La galvanisation des fils est un procédé de fabri cation intermédiaire entre la galvanisation au trempé et celles des tôles.
Les fils sont dits clairs (galvanisés en l'état écrouide tréfilage) ou recuits (galvanisés après recuit en ligne).
Pour certains usages les fils sont retréfilés aprèsgalvanisation.
D'une façon générale, la fabrication des pièces réalisées à base de fils se fait par pliage, torsion, enroulement, ce qui impose une bonne adhérence et aptitude à la déformation du revêtement sans écaillage. La norme NFA 91-131 donne trois classes de qualité pour les fils galvanisés :
– CLASSE A : Galvanisation ordinaire (pas d'exigence particulière en charge de zinc ou en continuité de revêtement).
– CLASSE B : Galvanisation soignée (charge minimale, continuité, adhérence).
– CLASSE C : Galvanisation épaisse (charge de zinc nettement plus forte, 2 à 3 fois par rapport à la classe B).
5. Caractéristiques et Normes :
5.1. Normes, masse et épaisseur :
Les masses et épaisseurs sur divers produits galvanisés sont données par le tableau ci-après :
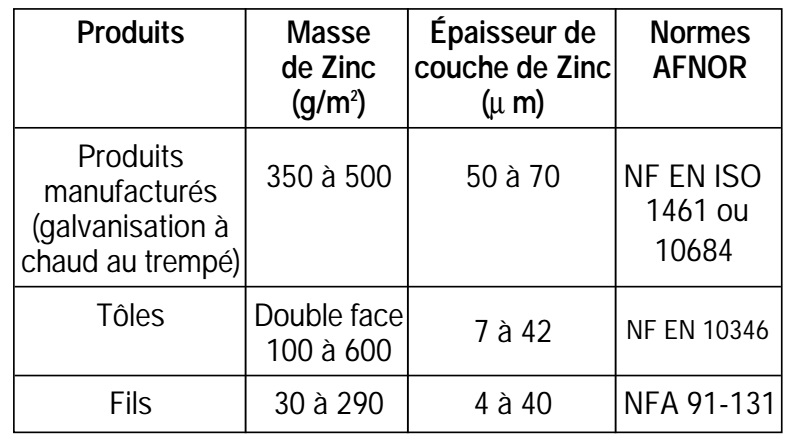
5.2. Découpage des tôles :
Pour les tôles galvanisées dont I'épaisseur totale ne dépasse pas 3 mm, les tranches mises à nu par le découpage restent insensibles à la corrosion grâce à l'effet de protection cathodique de l'acier par le zinc.
5.3. Contact avec d'autres matériaux :
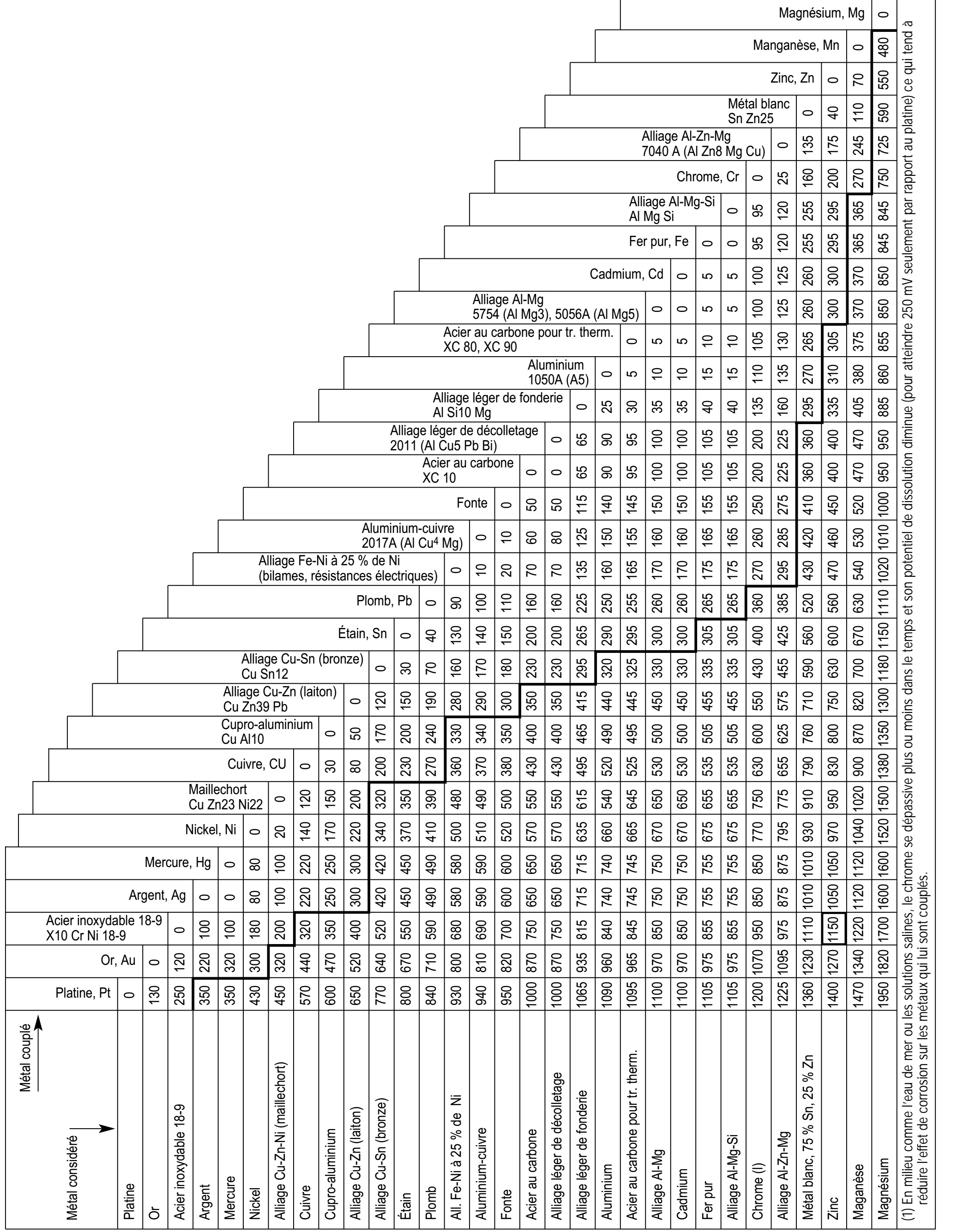
– Il faut éviter un contact direct avec d'autres métaux en milieu humide plus électropositifs que le zinc (par exemple le cuivre ou l'inox), car une rapide consommation du zinc par couplage galvanique aura lieu ; (Voir tableau page suivante.)
– des incompatibilités ont été signalées entre le zinc et les éléments de type acides, alcools, lubrifiants...
ANNEXE : Corrosion dues aux couples électrochimiques entre les matériaux et/ou revêtements d’un assemblage
Les différences de potentiel sont établies dans une solution aqueuse à 2 % de chlorure de sodium (NaCl), et exprimées en millivolts. En dessous de la ligne en trait fort, le métal en ordonnée est attaqué.
Notes :
– Le métal couplé ne subit pas de corrosion galvanique et bénéficie, au contraire, d’un effet de protection galvanique (faible si la différence de potentiel est petite, importante si la différence de potentiel est grande).
– L’effet galvanique est influencé par le rapport de surface des deux métaux :
• si la surface du métal considéré est la plus petite, sa corrosion augmente,
• si la surface du métal considéré est la plus grande, sa corrosion diminue.
Cet effet est d’autant plus accentué que la différence entre les deux surfaces est plus importante. (D’après NF E 25-032)